Moderne Behandlungsmöglichkeiten der Parodontitis
 Medizinische Expertise: Dr. med. Nonnenmacher
Medizinische Expertise: Dr. med. NonnenmacherQualitätssicherung: Dipl.-Biol. Elke Löbel, Dr. rer. nat. Frank Meyer
Letzte Aktualisierung am: 19. September 2019Dieser Artikel wurde unter Maßgabe medizinischer Fachliteratur und wissenschaftlicher Quellen geprüft.
Sie sind hier: Startseite Behandlungen Moderne Behandlungsmöglichkeiten der Parodontitis
Parodontalerkrankungen stellen einen der Hauptgründe für Zahnverlust im Erwachsenenalter dar. Laut WHO ist eine deutliche Diskrepanz zwischen dem Behandlungsbedarf und den tatsächlich durchgeführten Therapien erkennbar. Bei rund 60 % der Bundesbürger über 40 Jahre bestehen Parodontopathien, welche umgehend behandelt werden sollten. Parodontitis wird im Erwachsenenalter häufiger zur Ursache von Zahnverlust als Karies.
Inhaltsverzeichnis |
Obligat anaerobe Bakterien verursachen Parodontose
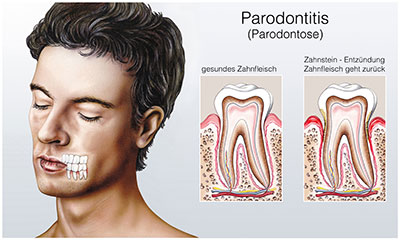
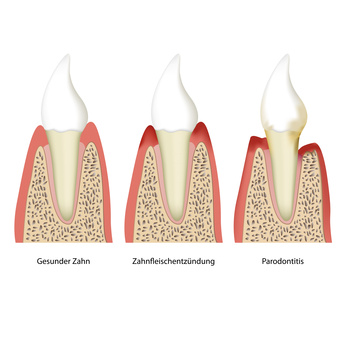
Unter der Parodontose versteht man die irreversible Entzündung des Zahnbettes, die zur Zerstörung von parodontalem Weich- und Knochengewebe führt, wie uns der auf Parodontologie spezialisierte Zahnarzt Dr. med. dent. Martin Hoppe M.Sc. erläuterte. Ursächlich dafür sind primär obligat anaerobe Bakterien, wie z.B. Porphyromonas gingivalis oder Treponema denticola. Fakultativ anaerobe Bakterien wie Aggregatibacter actinomycetem comitans verursachen alleine äußerst selten Parodontitis. Sie finden sich meistens in den Zahnfleischtaschen, wo sie als Zweitbesiedler von den Stoffwechselprodukten der aeroben Bakterien am Leben erhalten werden.
Fakultativ anaerobe Bakterien verbrauchen bei ihrem Stoffwechsel Sauerstoff, und sind so der Wegbereiter für die obligat anaeroben Bakterien, die eine sauerstofffreie Zone benötigen, um zu überleben. Somit ist auch die Anzahl der fakultativ anaeroben Bakterien in der Mundflora von Bedeutung. Je mehr davon vorhanden sind, desto bessere Lebensbedingungen werden für die aggressiven Drittbesiedler geschaffen, welche ihre Toxine freilassen. Die Reaktion des Körpers darauf ist das Freisetzen von proentzündlichen Zytokinen, welche die Entzündungsreaktion der Parodontitis verursachen.
Eine Mundflora, bei der sich die Keimverteilung im physiologischen Gleichgewicht befindet, setzt sich aus 25 % anaeroben Keimen und 75 % aeroben Keimen zusammen. Bei einer Parodontopathie sieht die Zusammensetzung genau umgekehrt aus. Die persönliche Zusammensetzung der Mundflora ist also ausschlaggebend für die Erkrankung an Parodontose. Bei einem stark ausgeprägten Immunsystem ist es durchaus möglich, dass die bakterielle Infektion so bekämpft wird, dass es trotz unzureichender Mundhygiene zu keiner Parodontopathie kommt.
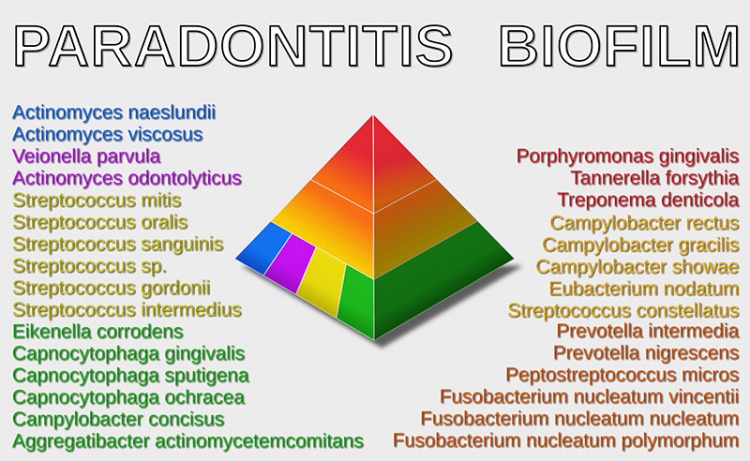
Die anschließende Infografik zeigt, aus welchen Bakterien sich der Biofilm von Parodontosepatienten zusammensetzt:
Die Entwicklung einer Parodontose wird noch von weiteren Faktoren bestimmt, wie beispielsweise:
- genetische Prädisposition,
- Rauchen,
- Diabetes,
- Erkrankungen, welche Immunschwäche mit sich bringen,
- Mangelernährung
Wann ist ein Keimtest zielführend?
Wie schwer der Mundraum von den krankmachenden obligat anaeroben Bakterien befallen ist, zeigt der Sondentest. Bei klinischer Inspektion fallen auch hohe Taschentiefen und Blutungen beim Sondentest ins Auge.
Zur genaueren Bestimmung stehen u.a. der Gram-Test und die Erregeranzucht zur Verfügung, wobei auf letztere aus Präzisionsgründen durchaus häufiger zurückgegriffen wird. Da der Bakterientest keine kassenspezifische Leistung ist, empfehlen wir ihn in unserer Praxis auch nur dann, wenn er wirklich sinnvoll ist, sagte uns Dr. Hoppe.
Folgende Indikationen sprechen für einen Bakterientest bei Parodontitis:
- Therapieresistente oder aggressive Erkrankungsverläufe
- Kinder oder Jugendliche als Betroffene
- Zahnfleischtaschen von mehr als 4 mm Tiefe
Für den Bakterientest erfolgt die Entnahme von Bakterienproben aus den tiefsten Zahnfleischtaschen. Für den Gram-Test werden die Proben getrocknet und mittels Einfärben mit basischem Farbstoff die Keime sichtbar gemacht. Einzelerreger bestimmen lassen sich mit dieser Methode allerdings keine. Dieser Vorgang erfolgt in molekularbiologischen Speziallabors durch Keimanzucht. Nach dem Ablauf von 24 Stunden kann man die verschiedenen Parodontose-Keime einzeln bestimmen.
Aggressive Parodontose als Indikator für Herzinfarkte?
Als häufigste Folgeerscheinung einer Parodontitis ist mit Zahnverlust zu rechnen. Unter anderem an den Universitäten von Dresden, Kiel, Amsterdam und Bonn wurde in der Vergangenheit jedoch nachgewiesen, dass ein Zusammenhang zwischen einer aggressiven Parodontoseerkrankung und dem Auftreten von Herzinfarkten besteht. Anscheinend ist eine Genveränderung auf Chromosom 9 im Gen ANRIL ursächlich. Dieses Gen kodiert den Forschungen zufolge ein regulatorisches RNA Molekül. Diese Moleküle haben aller Wahrscheinlichkeit nach einen Einfluss auf grundlegende physiologische Prozesse.
Am Institut für Molekularbiologie der Universität Kiel wurde eine eindeutige Übereinstimmung in der Genetik von Patienten mit aggressiver Parodontitis sowie Patienten mit einer Erkrankung der Herzkranzgefäße gefunden.
Diese genetische Übereinstimmung ist jedoch nicht der einzige Indikator, der für einen Zusammenhang von Parodontitis und Herzinfarkt spricht. Die hauptsächliche Ätiologie für Herzinfarkte in Deutschland bilden atheromatöse Plaques bzw. Thrombosen. In beiden Fällen kommt es zu einem Sauerstoffmangel im Herzen.
Studien zufolge wandern die Erreger der Parodontitis durch das arterielle System und verursachen auch an anderer Stellen Entzündungen. Diese Reaktionen führen zu einem Anschwellen der Gefäße, was einen reduzierten Blutfluss zur Folge hat und einen Herzinfarkt begünstigen kann. Vor allem das Bakterium Porphyromonas gingivalis wurde in den Thrombozyten von Herzinfarktpatienten nachgewiesen, wo es offenbar zur Verklumpung der Blutplättchen beitrug.
Im Zuge bakterieller Infektionen bildet die Leber in der Akutphase C-reaktives Protein, dies ist auch bei Parodontose-Patienten der Fall. Wie bekannt ist, erhöht auch dieses Protein das Risiko kardiovaskulärer Erkrankungen.
Bessere Lebensqualität durch qualifizierte Parodontosebehandlung
Sowohl um Zahnverluste zu vermeiden, als auch aufgrund des Zusammenhangs mit schwerwiegenden Erkrankungen wird der Behandlung der Parodontitis in der Zahnmedizin eine große Bedeutung zugemessen. Als Goldstandard gilt die minimalinvasive geschlossene Wurzelbehandlung, als Debridement oder Kürettage bezeichnet. Stellt sich diese als nicht wirkungsvoll heraus, kann ein minimalinvasiver parodontalchirurgischer Eingriff vorgenommen werden. So können beispielsweise auch Knochendefekte aufgefüllt werden. Um Knochenabbau und Knochendefekte zu detektieren, wird in der Praxis Dr. Hoppe ein 3D-Röntgen (DVT) herangezogen.
Das Spektrum der adjuvanten Therapiemaßnahmen reicht von medikamentösen Wirkstoffen, welche eine Reduktion der Entzündungen herbeiführen, bis hin zur antibakteriellen photodynamischen Therapie.
Die antibakterielle photodynamische Therapie erweist sich nicht nur in der Behandlung der Parodontose hilfreich, sondern auch bei der Therapie von:
- Periimplantitis,
- Karies,
- Infektionen im Wurzelkanal,
- oralen Pilzerkrankungen,
- Läsionen der Mundschleimhaut,
- implantologischen Eingriffen (z.B. Sofortimplantate),
- größere chirurgische Eingriffe (all on 4)
Bei der aPDT wird der Biofilm der betroffenen Bereiche mit einem Photosensitizer blau angefärbt und mit Niedrigenergielaser aktiviert. Die folgende photodynamische Reaktion führt zur Bildung von Singulettsauerstoff, der zytotoxisch wirkt. Diese Therapieform ist besonders wirksam, da man auch die mechanisch schwer erreichbaren Areale therapieren kann. Der Patient benötigt keine Anästhesie, die zytotoxische Reaktion ist völlig schmerzfrei. Diese Behandlungsmethode stellt auch eine geeignete Therapieform für Angstpatienten dar.
Eine weitere sanfte Behandlungsmöglichkeit, die direkt am Infektionsherd (in der Zahnfleischtasche) wirkt, ist das Einbringen eines Periochips. Der Periochip besteht aus Gelatine und enthält in hochkonzentrierter Form Chlorhexidin, die Membran hat die Maße von 4 x 5 mm. In 7 bis 10 Tagen löst sich der Chip komplett auf, hat aber bereits ein Wirkstoffdepot im erkrankten Gewebe angelegt. Die Wirksamkeit beträgt rund 3 Monate. Wo Spülungen und Lösungen nicht an den Bakterienherd heranreichen, kann der Periochip vor Ort gegen pathogene Keime wirken. Nebenwirkungen bei Chlorhexidin sind kaum bekannt.
Quellen
- Gängler, P., et al.: Konservierende Zahnheilkunde und Parodontologie. Thieme, Stuttgart 2010
- Gängler, P., Hoffmann, T., Willershausen, B., Schwenzer, N., Ehrenfeld, M. (Hrsg.): Konservierende Zahnheilkunde und Parodontologie. Thieme, Stuttgart 2010
- Ott, R., Vollmer, H.P., Krug, W.: Klinik- und Praxisführer Zahnmedizin. Thieme, Stuttgart 2003