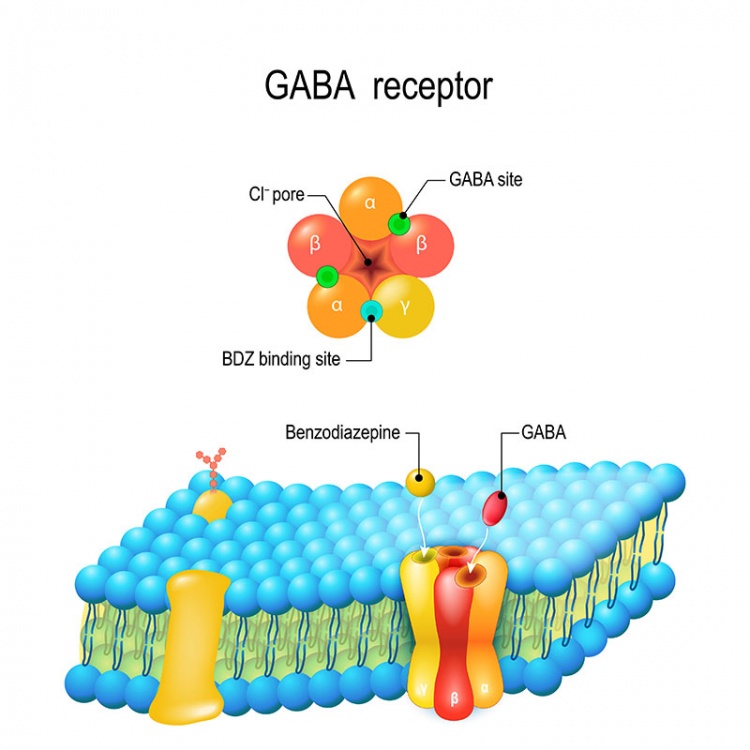
GABA-Rezeptor
 Medizinische Expertise: Dr. med. Nonnenmacher
Medizinische Expertise: Dr. med. NonnenmacherQualitätssicherung: Dipl.-Biol. Elke Löbel, Dr. rer. nat. Frank Meyer
Letzte Aktualisierung am: 7. März 2024Dieser Artikel wurde unter Maßgabe medizinischer Fachliteratur und wissenschaftlicher Quellen geprüft.
Sie sind hier: Startseite Anatomie GABA-Rezeptor
GABA-Rezeptoren sitzen im Nervensystem und binden an den Neurotransmitter γ-Aminobuttersäure. Durch die Bindung zeigen sie hemmende Wirkung auf Nervenzellen. Die gezielte Gabe von bestimmten Medikamenten kann die Rezeptoren und damit auch die Nervenzellen beeinflussen, was zum Beispiel für die Therapie von Epilepsie relevant ist.
Inhaltsverzeichnis |
Was ist ein GABA-Rezeptor?
Die Rezeptoren sind Sinneszellen, an die sich bestimmte Reize binden können. Rezeptoren sind in den Wahrnehmungsstrukturen zum Beispiel die erste Instanz jeder Wahrnehmung. Auch für viele andere Körperprozesse spielen diese Strukturen aber eine wichtige Rolle.
Das menschliche Nervensystem ist zum Beispiel mit GABA-Rezeptoren ausgestattet. An diese Rezeptoren binden sich die sogenannten Neurotransmitter. Diese Stoffe sind neurogen wirksame Substanzen und entsprechen damit Botenstoffen. Die Bindung der Botenstoffe an einem GABA-Rezeptor zeigt hemmende Wirkung auf die zugehörige Nervenzelle. Unterschieden werden ionotrope und metabotrope GABA-Rezeptoren. Zu den ionotropen Bindungsstellen zählt neben dem GABAA- vor allem der GABAC-Rezeptor.
Ein metabotroper Rezeptor ist der GABAB-Rezeptor. Die genaue Wirkungsweise von GABA-Rezeptoren hängt von der jeweiligen Untergruppe ab. Die ionotropen Varianten sind ligandengesteuert und wirken demnach auf den Ionen- und Elektrolythaushalt. Der Ioneneinstrom innerhalb einer Signalkaskade erfolgt zum Beispiel durch die Aktivierung von ionotropen GABA-Rezeptoren. Die metabotropen Rezeptoren wirken auf metabolische Vorgänge und aktivieren nach der Reizbindung die Bildung sekundärer Messengersubstanzen innerhalb der Signalkaskade.
Anatomie & Aufbau
Als Transmembrandomäne wird man die Lipid-Doppelschicht zur Durchspannung von integralen Membranproteinen bezeichnet. Rezeptoren sind mit Strukturen ausgestattet, an die sich bestimmte Substanzen binden können. Alle GABA-Rezeptoren reagieren aufgrund der festen Struktur ihrer Bindungsstellen ausschließlich auf spezifische Einflüsse und sind damit nur zur Bindung an bestimmte Botenstoffe oder Neurotransmitter in der Lage. Die Rezeptoren binden spezifisch vor allem den Neurotransmitter γ-Aminobuttersäure. Beim GABAB-Rezeptor handelt es sich anders als bei den anderen Untergruppen der GABA um einen G-Protein-gekoppelten Rezeptor, der sowohl prä-, als auch postsynaptisch sitzen kann.
GABAA-Rezeptoren entsprechen ligandenaktivierten Ionenkanälen, die für Hydrogen- und Chloridcarbonationen permeabel sind. Sie sind Heteropentamere und bestehen damit je aus fünf Untereinheiten, die die Zellmembran jeweils viermal durchspannen. Homologe Untereinheiten sind die sechs Vertreter α1 bis α6, die drei Vertreter β1 bis β3, die drei Vertreter γ1 bis γ3 und δ, ε, π oder θ mit je einem Vertreter. ρ besitzt drei Vertretern von ρ1 bis ρ3. Im Gehirn sind die Rezeptoren meist aus zwei α- sowie zwei β- und einer γ-Untereinheit aufgebaut. GABAA-Rezeptoren besitzen zusätzlich zur γ-Aminobuttersäure-Bindungsstelle allosterische Bindestellen, die auf Benzodiazepine ansprechen und an der γ-Untereinheit sitzen. An der β-Untereinheit sitzen Bindungsstellen für Neurosteroide und Barbiturate.
Funktion & Aufgaben
GABA-Rezeptoren sind entweder ligandengesteuert oder metabotrop. Zu den ligandengesteuerten Rezeptoren gehören die GABAA- und GABAC-Rezeptoren. Metabotrop ist nur der GABAB-Rezeptor. Der ligandengesteuerte GABAA-Rezeptor ist ein Chloridionenkanal. Wenn er an GABA bindet, strömt Cl- ein. Dieser Einstrom zeigt inhibitorische Wirkung auf die Nervenzelle. Im Gehirn sind diese Untervarianten weit verbreitet und sind für das Gleichgewicht zwischen der Erregung und der Dämpfung in den Nervenzellen verantwortlich.
Zentralnervös dämpfende Wirkstoffe wie Benzodiazepine, Propofol oder Antiepileptika binden an diesen Rezeptoren. Der ligandengesteuerte GABAA-ρ-Rezeptor lässt sich nicht durch Bicucullin hemmen. Damit zeigen Wirkstoffe wie Antiepileptika kaum Wirkung an diesen Stellen. Der metabotrope GABAB-Rezeptor findet sich entweder präsynaptisch oder postsynaptisch. Bei einer GABA-Bindung an präsynaptischen Rezeptoren strömt vermehr K+- ein. Der Einstrom von Ca2+ vermindert sich. Dadurch kommt es zur Hyperpolarisation: die Transmitterfreisetzung wird so gehemmt.
Bei einer Bindung an die postsynaptische Variante wird ein verstärkter K+-Einstrom aktiviert. Auf diese Weise entsteht das inhibitorisch postsynaptisches Potential. Diese Art der GABA-Rezeptoren ist für Substanzen wie das Muskelrelaxan Baclofen empfänglich. GABAA-Rezeptoren sind zusammenfassend im Gehirn und Rückenmark verbreitet, wo sie die mitunter wichtigste Rezeptoren zur Inhibition des zentralen Nervensystems sind. In den Basalganglien und im Kleinhirn sind diese Rezeptoren an der motorischen Kontrolle beteiligt.
Im Thalamus helfen die Rezeptoren bei der Einleitung und der Aufrechterhaltung von Schlaf. Im Rückenmark sitzen GABA-Rezeptoren auf den Motoneuronen, wo sie an der Reflexverschaltung und der Koordination von Bewegungen beteiligt sind.
Krankheiten
Alkoholika binden an die GABAA-Rezeptoren und verstärken an der Nervenzellmembran die Permeabilität für Chlorid-Ionen. Dadurch kommt es zur Hyperpolarisation und die Aktionspotenzialfrequenz nimmt ab. Weil das exzitatorische System per wegen der Bindung des Alkohols an NMDA-Rezeptoren gleichzeitig eine Hemmung erfährt, zeigt Alkohol auf den Menschen sedierende Wirkung. Dieser Zusammenhang kann bei Alkoholvergiftungen relevant sein und ist außerdem ein wichtiger Zusammenhang bei der klinischen Praxis an chronisch Alkoholsüchtigen.
Davon abgesehen lässt sich der Zustand des zentralen Nervensystems durch pharmakologische Substanzen beeinflussen, die zur Bindung an die GABA-Rezeptoren fähig sind. Das spielt in der klinischen Praxis bei der Behandlung von verschiedenen, neurologischen Erkrankungen eine wichtige Rolle. Die Behandlung von Epilepsie baut zum Beispiel auf diesem Zusammenhang auf, aber auch generell ist die gezielte Beeinflussung des Nervensystems durch die Gabe von Medikamenten ein Hauptbestandteil der Therapie. Tranquilizer wie Benzodiazepine wirken sedativ. Dasselbe gilt für Barbiturate, mit denen oft die Anästhesie eingeleitet wird.
Antiepileptika wie Valproat verhindern durch Hemmung der Rezeptoren epileptische Anfällen. Tiagabin hemmt die Wideraufnahme von GABA und erhöht die Konzentration im synaptischen Spalt, sodass epileptische Anfälle vermindert werden. Viele Medikamente wirken außerdem stimulierend auf GABAA-Rezeptoren und können damit Süchte auslösen. Die Sucht wird über α1-haltige Rezeptoren vermittelt. Ihre Reizung bewirkt in neuroplastischen Prozessen funktionelle Veränderungen bestimmter AMPA-Rezeptoren des jeweiligen Neurons.
Typische & häufige Erkrankungen des zentralen Nervensystems
Quellen
- Frotscher, M., et al.: Taschenatlas Anatomie, Band 3: Nervensystem und Sinnesorgane. Thieme, Stuttgart 2018
- Piper, W.: Innere Medizin. Springer, Berlin 2013
- Zilles, K. et al.: Anatomie. Springer Medizin Verlag Heidelberg 2010