Glutathion
 Medizinische Expertise: Dr. med. Nonnenmacher
Medizinische Expertise: Dr. med. NonnenmacherQualitätssicherung: Dipl.-Biol. Elke Löbel, Dr. rer. nat. Frank Meyer
Letzte Aktualisierung am: 15. März 2024Dieser Artikel wurde unter Maßgabe medizinischer Fachliteratur und wissenschaftlicher Quellen geprüft.
Sie sind hier: Startseite Laborwerte Glutathion
Glutathion (TSH) ist ein Tripeptid, bestehend aus den drei Aminosäuren Cystein, Glycin und Glutaminsäure. Glutathion gilt als eins der wichtigsten Antioxidantien im menschlichen Körper.
Inhaltsverzeichnis |
Was ist Glutathion?
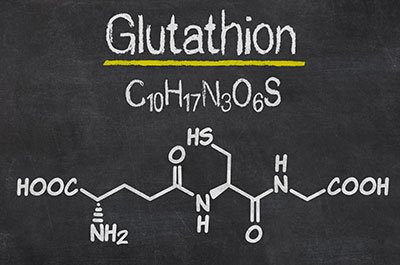
© Zerbor – stock.adobe.com
Glutathion wird auch als γ-L-Glutamyl-L-cysteinylglycin bezeichnet. Es ist ein schwefelhaltiges Tripeptid, gehört also zur Gruppe der Eiweiße.
Chemisch betrachtet handelt es sich bei Glutathion nicht um ein reguläres Tripeptid, da Glutaminsäure und Cystein über die γ-Carboxylgrupp der Glutaminsäure verbunden sind. Bei einem echten Tripeptid würde die Bindung über die α-Carboxylgruppe ausgebildet werden. Glutathion kommt im Körper als aktives, reduziertes Glutathion und als oxidiertes Glutathion vor. Hauptsächlich dient Glutathion als Cystein-Reserve und als Redox-Puffer.
Funktion, Wirkung & Aufgaben
Der Körper produziert zwar größere Mengen Cystein selber, da die Aminosäure aber durch Oxidation ständig und unwiderrufbar verloren geht, kann es zu Mangelzuständen kommen. In diesem Fall kann Glutathion in Cystein umgewandelt werden. Im Blut zirkulieren etwa drei Gramm Cystein in Form von Glutathion. Dieser Vorrat reicht für drei Tage. Auch zur Taurinsynthese kann Glutathion genutzt werden. Taurin spielt eine Rolle bei der Produktion von Gallensäuren und beeinflusst die Signalübertragungen im Zentralnervensystem. Taurinmangel führt zu Immunschwäche und Störungen im Immunsystem.
Eine weitere wichtige Aufgabe von Glutathion ist der Schutz von Proteinen und Membranlipiden vor sogenannten freien Radikalen. Freie Radikale entstehen bei zahlreichen Stoffwechselprozessen, die unter Sauerstoffverbrauch ablaufen. Auch durch äußere Faktoren wie Stress, Ozon, UV-Strahlung, Nahrungsmittelzusatzstoffe und zahlreiche Chemikalien entstehen im Körper freie Radikale.
Die kurzlebigen Moleküle können die DNA und die RNA der Zellen, Eiweiße und Fette schädigen. Freie Radikale spielen eine Rolle im Alterungsprozess und bei der Entstehung vieler Krankheiten wie Krebs, Arteriosklerose, Diabetes mellitus oder Alzheimer. Um die Zellen vor den freien Radikalen zu schützen, wird Glutathion oxidiert. Darüber hinaus hilft Glutathion der Leber dabei Schad- und Giftstoffe auszuscheiden.
Bei jedem schädlichen Molekül, das ausgeschieden werden soll, ist unter anderem Glutathion erforderlich. Es schwächt die schädliche Wirkung von Röntgenstrahlung und Chemotherapie. Auch die Wirkungen von Tabakrauch und Alkohol kann Glutathion abmildern. Glutathion wird auch genutzt zur Entgiftung bei Intoxikationen mit Schwermetallen wie Blei, Cadmium oder Quecksilber. Das Tripeptid sichert zudem den physiologischen Ablauf von Zellteilung, Zelldifferenzierung und Zellstoffwechsel und verhindert im besten Fall damit Entartungen. Glutathion übernimmt zudem Aufgaben im Immunsystem. So ist es an der Bildung sogenannter Leukotriene beteiligt. Diese steuern die weißen Blutkörperchen. Glutathion dient somit auch der Stärkung des Immunsystems.
Bildung, Vorkommen, Eigenschaften & optimale Werte
Eigentlich sind fast alle Zellen im Körper in der Lage Glutathion herzustellen. Hauptproduktionsort ist aber die Leber. Zur Bildung werden Cystein, Glycin und Glutaminsäure, Adenosintriphosphat (ATP) und Magnesiumionen benötigt.
Aber auch in Lebensmitteln, insbesondere in Obst und Gemüse, ist Glutathion enthalten. Einen hohen Gehalt an Glutathion haben Wassermelonen, Spargel, Orangen, Brokkoli, Zucchini, Spinat oder Kartoffeln. Nahrungsmittel, die Limonen enthalten, sind förderlich für die Synthese eines Enzyms, welches Glutathion enthält. Limonene sind in Sellerie, Fenchel, Soja oder Weizen enthalten. In der Regel wird der Bedarf an Glutathion durch eine ausgewogene Ernährung gedeckt, sofern sie ausreichend Cystein, Glutaminsäure, Magnesium und Selen beinhaltet.
Im Körper kommt Glutathion in zwei Formen vor. Zum einen liegt es als aktives, reduziertes Glutathion vor und zum anderen als oxidiertes Glutathion. Bei einem gesunden Menschen beträgt das Verhältnis von aktivem zu oxidiertem Glutathion 400:1. Das aktive Glutathion ist die wirksame Form. Nur in dieser Form ist das Tripeptid in der Lage freie Radikale unschädlich zu machen.
Krankheiten & Störungen
Luft- und Wasserverschmutzung, verschreibungspflichtige Medikamente, Verletzungen, Verbrennungen, Traumata, Schwermetallvergiftungen, radioaktive Bestrahlung, Autoabgase, chemische Reinigungsmittel und alle Vorgänge, die im Körper freie Radikale erzeugen, sorgen für einen verstärkten Abbau von Glutathion und somit eventuell für einen Glutathion-Mangel. Eigentlich handelt es sich nicht um einen generellen Mangel an Glutathion, sondern vielmehr um einen Mangel an reduziertem aktivem Glutathion. Um Schäden auszugleichen und die freien Radikale abzuwehren, verbraucht der Körper die aktive Form.
Eigentlich regeneriert das Enzym Glutathion-Reduktase die oxidierte Form und bringt sie wieder in die aktive Form zurück. Ist jedoch die Belastung im Körper durch Gifte, Schadstoffe und freie Radikale zu groß, kann das Enzym seine Aufgabe nicht mehr komplett erfüllen und es bleibt vermehrt oxidiertes Glutathion zurück. Das gesunde Verhältnis von 400:1 ist nicht mehr gewährleistet. Unter diesen Umständen kann das Glutathion-Redoxsystem nicht mehr richtig funktionieren. Damit ist auch die Funktion der antioxidativen Abwehr stark beeinträchtigt.
Eine Konsequenz daraus ist, dass die Mitochondrien in den Zellen nicht mehr ausreichend Adenosintriphosphat produzieren können. ATP ist der wichtigste Energiespeicher und Energielieferant im Stoffwechsel und wird bei sämtlichen Stoffwechselvorgängen benötigt. Ohne ausreichend ATP kommt es zu einem Energiedefizit. Chronische Müdigkeit ist die Folge. Bei vielen Erkrankungen ist der Glutathion-Spiegel erniedrigt. Insbesondere in der biologischen Krebstherapie wird deshalb immer öfter adjuvant zur Chemotherapie und zu Bestrahlungen Glutathion verordnet.
Quellen
- Gerok, W., Huber, C., Meinertz, T., Zeidler, H. (Hrsg.): Die innere Medizin – Referenzwerk für den Facharzt. Schattauer, Stuttgart 2007
- Löffler, G.: Basiswissen Biochemie. Springer, Berlin 2008
- Schänzler, N., Bieger, W.P.: Laborwerte. Gräfe und Unzer, München 2009
