Lysosomale Speicherkrankheit
 Medizinische Expertise: Dr. med. Nonnenmacher
Medizinische Expertise: Dr. med. NonnenmacherQualitätssicherung: Dipl.-Biol. Elke Löbel, Dr. rer. nat. Frank Meyer
Letzte Aktualisierung am: 15. März 2024Dieser Artikel wurde unter Maßgabe medizinischer Fachliteratur und wissenschaftlicher Quellen geprüft.
Sie sind hier: Startseite Krankheiten Lysosomale Speicherkrankheit
Insgesamt sind 45 verschiedene lysosomale Speichererkrankungen, bei denen es sich um eine heterogene Gruppe angeborener Stoffwechselerkrankungen handelt, bekannt. Menschen, die unter einer dieser Erkrankungen leiden, weisen einen genetischen Defekt auf. Alle Speicherkrankheiten haben eines gemeinsam: ein bestimmtes Enzym ist nicht vorhanden oder nur zum Teil funktionsfähig.
Inhaltsverzeichnis |
Was ist eine lysosomale Speicherkrankheit?
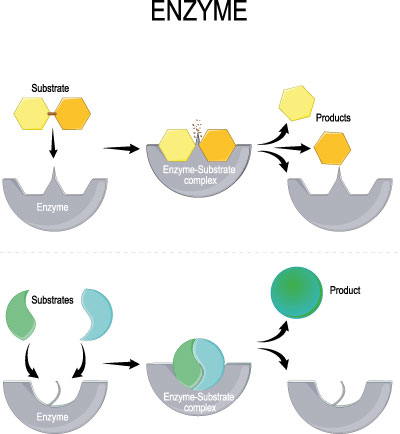
© designua – stock.adobe.com
Diese angeborenen Speicherkrankheiten treten nur selten auf, da weniger als fünf von 10.000 Menschen betroffen sind. Die verschiedenen Erkrankungen verlaufen sehr verschieden, die Symptome können stark variiert auftreten.
Die bekanntesten Formen der lysosomalen Speicherkrankheit sind Morbus Fabry, Morbus Gaucher, Morbus Pompe und Mukopolysaccharidose (MPS). Sie werden häufig auch als „Waisenkinder der Medizin“ bezeichnet, weil der Weg zu einer konkreten Diagnose und einer geeigneten Therapie sehr lang sein kann. Zuweilen können Jahre vergehen bis die Betroffenen erfahren, was mit ihnen geschieht.
Ursachen
Enzyme haben die Aufgabe, Schad- und Abfallstoffe, die sich im menschlichen Organismus über den Stoffwechsel ansammeln über die Lysosome zu entsorgen, beziehungsweise diese wieder so aufzuarbeiten, dass Beschwerden ausbleiben.
Liegt ein Enzymmangel vor, ist dieser reibungslos funktionierende Entsorgungskreislauf nicht mehr gewährleistet. Die schädlichen Stoffe setzen sich in den Zellen ab und stören den Stoffwechselkreislauf. In der Anfangsphase wirken sich die Störungen noch nicht merklich aus, es bestehen nur wenige Einschränkungen. Bleibt diese Stoffwechselwechselerkrankung als Folge eines Enzymmangels jedoch unbehandelt, vervielfachen sich die Beschwerden, da es zu einer starken Vergrößerung der Zellen kommt.
Symptome, Beschwerden & Anzeichen
Im schlimmsten Fall gehen diese unter. Die Folgen sind Schädigungen der Knochen, des Nervensystems, Milz, Nieren, Muskeln oder Herz. Morbus Fabry sorgt aufgrund der verminderten oder fehlenden Enzymtätigkeit für eine Fetteinlagerung (Globotriaosylceramide, Gb3) in den Zellen. Diese unerwünschten Ablagerungen können zu starken Schmerzzuständen in den Zehen oder Fingern, Hirnschlag und Nierenschädigungen führen.
Diagnose & Krankheitsverlauf
Dieses Krankheitsbild betrifft verschiedene Systeme gleichzeitig: Blutgefäße, Nieren, Herz und Nervensystem. Die autosomal-rezessiv vererbte Morbus-Gaucher-Erkrankung verursacht eine Mutation des Enzyms „Beta-Glukozerebrosidase“ und führt zu einer Akkumulation von Substrat innerhalb der Zellen, besonders in den Makrophagen (Fresszellen), die zum retikulo-endothelialen System gehören. Das Blutbild verändert sich, Leber und Milz sind vergrößert und die Knochen schmerzen.
Die Erkrankung verläuft progredient und ist meistens ethnisch bedingt, da sie in den meisten Fällen bei Menschen jüdischer Abstammung auftritt. Morbus Pompe ist auch als „Saure-Maltase-Mangel“ bekannt. Das Krankheitsbild gehört in die Gruppe der Glykogenesen Typ II. Den betroffenen Personen fehlt das Enzym „Alpha-1,4-Glucosidase“ (Saure Maltase) beziehungsweise es ist in nicht ausreichender Menge vorhanden. Patienten leiden aufgrund des gestörten Glykogenabbaus in den Muskeln unter einer Zerstörung der Muskelzellen in Form von Zuckereinlagerung.
Der Mukopolysaccharidose Typ I (MPS), auch als Morbus Hunter bezeichnet, führt zu verschiedenen klinischen Ursachen. Morbus Hurler ist die schwerste Verlaufsform und Morbus Scheie befindet sich am Schluss der klinischen Patogenese. Zwischen diesen beiden Verlaufsformen stehen Übergänge unterschiedlicher Ausprägung. Die hervorstechende Eigenschaft ist der gestörte Abbau von Kohlenhydraten, die sich in den Lysosomen der Zellen anreichern.
Morbus-Hunter-Patienten können unter Minderwuchs, vergrößerter Milz und Leber, groben Gesichtszügen, verdickter Haut, vergrößerter Zunge und Atemproblemen leiden. Zudem ist das Skelett häufig im Bereich von Becken, Wirbelsäule, Handknochen und Schädel verändert. Nabel- und [[Leistenbrüche] sind möglich.
Komplikationen
Davon sind vor allem die Nieren, die Leber und die Milz betroffen. Auch das Herz kann von dieser Erkrankung betroffen sein, sodass es im schlimmsten Falle zum Herztod kommt. Weiterhin treten auch Schädigungen an den Nieren auf und die Betroffenen leiden nicht selten an Schmerzen an den Zehen oder Fingern. Auch Lähmungen können dabei auftreten, wenn das Gehirn durch diese Krankheit geschädigt wurde. Die Leber und die Milz können vergrößert sein und ebenso zu starken Schmerzen führen.
Nicht selten sind die Knochen des Betroffenen brüchig und schmerzen ebenfalls. Die Behandlung dieser Krankheit erweist sich als schwierig. In vielen Fällen ist die Lebenserwartung des Betroffenen dabei deutlich verringert. Bei der Behandlung mit Medikamenten kommt es in der Regel nicht zu besonderen Komplikationen. Ein positiver Krankheitsverlauf kann allerdings nicht in jedem Fall garantiert werden.
Wann sollte man zum Arzt gehen?
Haarausfall, Gelenkbeschwerden und Organstörungen sind mögliche Anzeichen einer lysosomalen Speicherkrankheit. Ein Arztbesuch empfiehlt sich, wenn die Beschwerden immer wieder auftreten oder sich ganz plötzlich einstellen, ohne dass eine Ursache dafür zu finden ist. Wenn die Symptome im Zusammenhang mit einem bereits diagnostizierten Enzymdefekt oder einer anderen schweren Erkrankung auftreten, muss der zuständige Arzt konsultiert werden. Eine unbehandelte Speicherkrankheit kann zu Demenz, Unfruchtbarkeit, Neuropathien und anderen, zum Teil lebensbedrohlichen Komplikationen führen. Deshalb sollten alle denkbaren Krankheitszeichen untersucht werden, auch wenn noch kein konkreter Verdacht besteht.
Die Symptome einer lysosomalen Speicherkrankheit können in Phasen auftreten oder sich schleichend entwickeln, bedürfen aber immer einer Untersuchung und Behandlung. Betroffene Personen sprechen am besten direkt mit dem Hausarzt oder einem Internisten. Die eigentliche Therapie erfolgt meist in einer Fachklinik für innere Erkrankungen, wobei je nach Symptombild eine Physiotherapie oder Psychotherapie angeschlossen sein kann. Insbesondere therapeutische Maßnahmen sind aufgrund des oftmals negativen Verlaufs der Erkrankung angezeigt.
Behandlung & Therapie
Je nachdem wie früh eine adäquate Diagnose gestellt wird, sind diese Erbkrankheiten durch eine Enzymersatztherapie sehr gut zu behandeln, so dass die betroffenen Personen wesentlich weniger Beschwerden haben und damit mehr Lebensqualität. Diese Ersatztherapie wird entsprechend des Krankheitsbildes eingesetzt.
Menschen, die unter Morbus Gaucher leiden, fehlt das „Enzym ß-Glukozerebrosidase“, das biotechnologisch hergestellt und dem Organismus des Patienten mittels Infusion zuführt wird. Lysosomen agieren effizient und sind in der Lage, Stoffe aus ihrer unmittelbaren Umgebung aufzunehmen. Aus diesem Grund sind die künstlich eingesetzten Enzyme derart modifiziert, dass sie den Lysosomen auf ideale Weise zugeführt werden können.
Die Makrophagen (Fresszellen) bauen die in den Zellen angereicherten Glukozerebroside ab. Diese Therapie lässt sich mit der Insulintherapie bei Diabetes mellitus vergleichen, mit dem Unterschied, dass nicht ein fehlendes Hormon, sondern ein nicht vorhandenes Enzym zugeführt wird. Der Körper baut alle Substanzen regelmäßig ab, so auch das zugeführte künstliche Enzym.
Aufgrund dieses regelmäßigen Substanzabbaus müssen sich die Patienten dieser Infusionstherapie regelmäßig bis zum Lebensende unterziehen. Die Enzymersatztherapie greift nicht symptomatisch, sondern bekämpft direkt die Ursache der Erberkrankung. Mediziner bezeichnen diese Therapie als kausal. Die Therapiegrundsätze sind für alle vier zuvor genannten häufigen Speichererkrankungen anzuwenden.
Auch Pompe-Patienten werden mittels einer Infusionstherapie behandelt. Bei dieser Erkrankung wird das nicht existente Enzym „saure Alfa Glukosidase“ zugeführt und ist dabei behilflich, Glykogen abzubauen, das sich in den Lysosomen der Muskeln angereichert hat. Bei Patienten mit dem Krankheitstyp „Mukopolysaccharidose Typ I“ ist das lysosomale Enzym „alpha-Iduronidase“ nicht oder in nicht ausreichender Mange vorhanden. Es handelt sich um eine der seltensten Speicherkrankheiten, bei der sich Zuckermoleküle in den Organen und im Gewebe anreichern.
Bei normalem Verlauf baut das Enzym Mukopolysacchariden ab. Die Zuckermoleküle sind langkettig und am Aufbau von Stütz- und Bindegewebe, zum Beispiel Knochen, Haut, Gelenkflüssigkeiten und Knorpel, beteiligt. Wird der normal verlaufende Abbau aufgrund des fehlenden Enzyms gestört, reichern sich krankhafte Glykosaminoglykane (GAG) in den einzelnen Zellen an. Zukünftige Therapie-Optionen zielen auf die Einnahme von Tabletten ab.
Aussicht & Prognose
Die Prognose der Speicherkrankheit ist ungünstig. Als Ursache der gesundheitlichen Störung wurde eine genetische Disposition festgestellt. Rechtliche Vorgaben untersagen es Medizinern und Wissenschaftlern, die menschliche Genetik zu verändern. Aus diesem Grund bleibt die Erkrankung lebenslang erhalten und hat keine Aussicht auf eine Genesung.
Der behandelnde Arzt konzentriert sich auf die Therapie der entstehenden Symptome. Unbehandelt kommt es über die Lebenszeit zu einer Zunahme verschiedener Beschwerden. Das Knochensystem wird geschädigt und Probleme der Organe treten auf. Im schlimmsten Fall kommt es zu Funktionsschwierigkeiten der inneren Organe und letztlich zu einem Ausfall der Organtätigkeit. Damit droht dem Betroffenen das vorzeitige Ableben.
Die Herausforderung der Erkrankung liegt in der Diagnosestellung. Bei einer Vielzahl der Patienten treten nennenswerte und stark wahrnehmbare Beschwerden erst im späteren Verlauf des Lebens auf. Dadurch bleibt über lange Zeit die Genstörung unbemerkt und eine frühe Behandlung der Erkrankung ist erschwert. Je später eine Diagnose gestellt wird, desto ungünstiger ist der weitere Verlauf. In einem fortgeschrittenen Krankheitsstadium sind die inneren Organe oder die Gelenke bereits stark geschädigt. Operative Eingriffe werden benötigt und bei einem ungünstigen Krankheitsverlauf kann nur ein Spenderorgan das Leben des Betroffenen retten. Daher ist für eine verbesserte Prognosestellung eine frühe Behandlung essenziell.
Vorbeugung
Da es sich um einen angeborenen Gendefekt handelt, der die Ausprägung eines Enzyms verhindert, ist diese Erkrankung präventiv nicht behandelbar. Allerdings könnten neueste Errungenschaften der Gentechnik auf diesem Feld einen Ansatz liefern.
Nachsorge
Bei dieser Krankheit leiden die Betroffenen an einer Reihe von verschiedenen Komplikationen und Beschwerden. Diese wirken sich in der Regel alle sehr negativ auf die Lebensqualität des Betroffenen aus, sodass schon eine sehr frühzeitige Diagnose erfolgen sollte. Je früher dabei ein Arzt aufgesucht wird, desto besser ist meist auch der weitere Verlauf bei dieser Erkrankung.
Die Ausprägung dieser Krankheit kann sehr unterschiedlich sein, sodass eine allgemeine Voraussage oftmals nicht möglich ist. Die Betroffenen leiden an starken Schäden der inneren Organe. Damit sind die Nieren und das Herz in erster Linie betroffen, sodass das Kind schon in erster Tagen versterben kann, wenn die Beschwerden nicht rechtzeitig korrigiert werden. Ebenso kommt es an unterschiedlichen Stellen des Körpers zu Ablagerungen von Fett.
Dabei sind vor allem die Finger und Zehen betroffen, was zu einer deutlich verringerten Ästhetik des Betroffenen führen kann. In der Regel kommt es im weiteren Verlauf zu Schädigungen der Nieren und des Gehirns, sodass der Betroffene an den Folgen dieser Schäden verstirbt. Auch die Eltern und die Angehörigen leiden aufgrund der Erkrankung häufig an Depressionen oder an anderen psychischen Verstimmungen.
Das können Sie selbst tun
Lysosomale Speicherkrankheiten bedürfen sehr häufig einer intensiven medizinischen Betreuung. Oft gibt es keine ausreichenden Selbsthilfemöglichkeiten. Die Eltern von betroffenen Kindern erleben häufig schwere Belastungen im häuslichen Umfeld, weil ihr Kind ständige Betreuung und Pflege benötigt.
Die Krankheitsbilder der einzelnen Speicherkrankheiten sind unterschiedlich. Es gibt sowohl leichte als auch sehr schwere Formen. Ein Beispiel ist Morbus Gaucher. Die Hilfe der Eltern beschränkt sich oft nur auf die Fütterung des schwerbehinderten Kindes. In leichteren Fällen kann die Lebenserwartung fast normal sein. Trotzdem ist eine ständige ärztliche Überwachung notwendig, um mögliche Komplikationen abzuwenden. Eine regelmäßige körperliche Betätigung gehört zu den Begleittherapien, die auch zuhause durchgeführt werden können. Des Weiteren muss eine sorgfältige Krebsvorsorgeuntersuchung veranlasst werden. Das erfordert von den Eltern ständige Arztbesuche mit ihrem Kind. Gleiches gilt auch für andere lysosomale Speicherkrankheiten.
Bei manchen Erkrankungen können neben körperlichen Behinderungen auch geistige Einschränkungen auftreten, die noch einer besonderen Förderung bedürfen. Bei leichteren Verlaufsformen bestimmter Erkrankungen wie unter anderem bei Morbus Hunter treten anfangs nur Skelettveränderungen und Gesichtsdysmorphien auf. Hier ist der betroffene Patient oft aber zu einem eigenständigen Leben befähigt. Allerdings sind auch hier ständige ärztliche Untersuchungen erforderlich, um eventuelle Komplikationen wie Herzinsuffizienz oder Atemwegserkrankungen auszuschließen. Psychische Belastungen aufgrund der körperlichen Deformationen kann der Patient durch psychologische Beratung aufarbeiten.
Quellen
- Arasteh, K., et. al.: Innere Medizin. Thieme, Stuttgart 2013
- Herold, G.: Innere Medizin. Selbstverlag, Köln 2016
- Piper, W.: Innere Medizin. Springer, Berlin 2013
